면역항암제 치료 어려운 삼중음성 유방암 대상에서 PFS 개선 확인
정경해 교수 "두 연구 임상지침 바꿀 연구…환자에 따라 약제 결정"
[베를린=홍숙 기자] 지난 19일(현지시각) 독일 베를린에서 열린 유럽종양학회 연례학술대회(ESMO 2025)에서 난공불락 삼중음성 유방암 관련 박수갈채를 받는 연구 결과가 잇달아 발표됐다.
주인공은 트로델비(성분명 사시투주맙 고비테칸)와 다트로웨이(성분명 다토포타맙데룩스테칸, Dato-DXd). 이 자리에선 삼중음성 유방암을 대상으로 한 트로델비 3상 임상시험인 'ASCENT-03'와 다트로웨이 3상 'TROPION-Breast02' 연구가 발표됐다.

먼저 ASCENT-03 결과, 삼중음성 유방암환자의 1차 치료에서 트로델비가 기존 항암화학요법(chemotherapy) 대비 무진행생존기간(Progression-Free Survival, PFS)을 유의하게 개선한 것으로 나타났다.
ASCENT-03은 PD-(L)1 억제제 치료가 적합하지 않은 국소 진행성 불응성 또는 전이성 삼중음성유방암 환자를 대상으로 트로델비와 표준 화학요법을 직접 비교한 3상 연구다.
연구에는 총 558명의 환자가 등록돼 일대일 비율로 트로델비(10mg/kg, 21일 주기 1·8일 투여)군과 화학요법군(파클리탁셀·나브파클리탁셀·젬시타빈/카보플라틴 병용 중 선택)으로 무작위 배정됐다.
주요 평가변수는 PFS였으며, 전체생존율(Overall Survival, OS), 객관적반응률(Objective Response Rate, ORR), 반응지속기간(Duration of Response, DOR) 등이 주요 2차 평가변수로 설정됐다.
그 결과, 트로델비는 화학요법 대비 PFS를 유의하게 개선했다. mPFS는 트로델비 군이 9.7개월로 대조군 6.9개월 대비 사망 또는 질병 진행 위험을 38% 감소시켰다(위험비: 0.62).
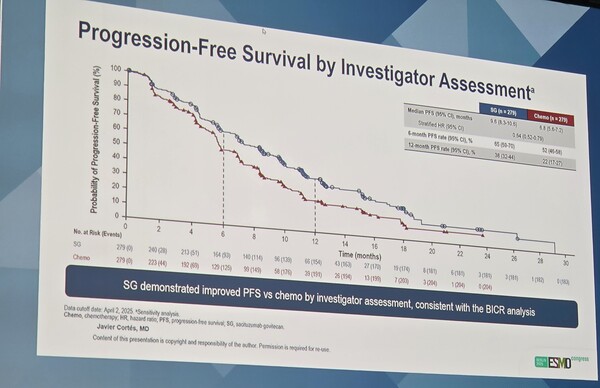
전체생존율(OS)은 아직 성숙하지 않았으나, 중간 분석에서 두 군 간 중앙값 OS는 트로델비 군이 21.5개월로, 대조군 20.2개월과 유사한 양상을 보였다. 반면 2차 무진행생존기간(PFS2)은 트로델비군이 화학요법군보다 4.2개월 더 길게 유지됐다.
안전성 측면에서도 트로델비는 기존 데이터와 일관된 결과를 보였다. 가장 흔한 이상반응은 호중구감소증(67%), 구역(61%), 탈모(56%), 설사(47%), 피로(47%) 등이었으며, 3등급 이상 이상반응 발생률은 화학요법군보다 낮았다. 예방적 G-CSF 사용은 권장됐으며, 치료 중단율 역시 트로델비군에서 낮게 나타났다.
뒤이어 다트로웨이 3상인 'TROPION-Breast02' 연구도 공개됐다. 해당 연구는 국소 진행성 불응성 또는 전이성 삼중음성유방암 환자 중, 이전에 전이성 치료를 받은 적이 없고 면역항암제 치료가 적합하지 않은 환자 644명을 대상으로 진행됐다.

환자들은 일대일 비율로 다토-DXd(6mg/kg, 3주 간격 정맥주사)군과 연구자 화학요법(Investigator’s Choice Chemotherapy, ICC; 파클리탁셀, 나브파클리탁셀, 에리불린, 카보플라틴, 카페시타빈 중 선택)군으로 무작위 배정됐다.
주요 평가변수는 PFS와 OS로 설정됐으며, 중간 추적기간은 27.5개월이었다. 분석 결과, Dato-DXd는 화학요법 대비 PFS와 OS 모두에서 통계적으로 유의하고 임상적으로 의미 있는 개선을 보였다.
mPFS는 각각 Dato-DXd군이 10.8개월(95% CI 8.8–13.0)로 대조군 5.6개월(95% CI 5.0–7.0) 대비 길었고, 질병 진행 또는 사망 위험을 43% 감소시켰다(위험비 0.57; 95% CI 0.47–0.69; p<0.0001).
전체생존율(OS)에서도 유의한 개선이 관찰됐다. 중앙값 OS는 Dato-DXd군 23.7개월(95% CI 19.8–25.6), 화학요법군 18.7개월(95% CI 16.0–21.8)로, 사망 위험을 21% 낮췄다(위험비 0.79).
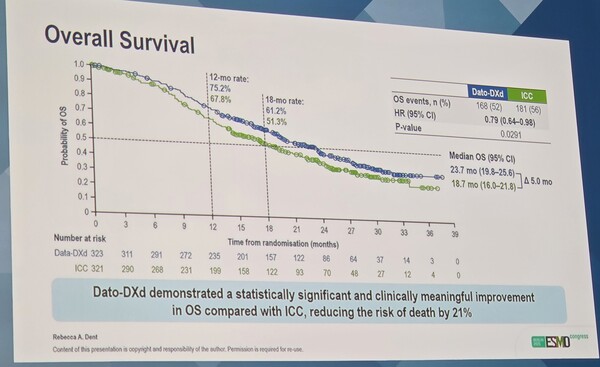
반응지속기간(Duration of Response, DoR)은 Dato-DXd군에서 12.3개월로, 화학요법군의 7.1개월 대비 약 5개월 이상 길었다.
안전성 측면에서도 다토-DXd는 예측 가능한 독성 프로파일을 보였다. 치료 관련 이상반응은 대부분 관리 가능했으며, 3등급 이상 이상반응 발생률은 Dato-DXd군 33%로, 화학요법군 29%dhk 유사했다.
주요 특이 이상반응으로는 구내염(25%), 안표면 질환(15%) 등이 보고됐으나 대부분 1~2등급으로, 90% 이상이 회복됐다. 간질성폐질환(ILD) 또는 폐렴 관련 사건은 1% 미만에서 보고됐다.
현장에서 만난 서울아산병원 종양내과 정경해 교수는 "두 연구는 삼중음성 유방암의 임상지침을 바꿀 수 있는(‘practice-changing) 연구 결과"라며 "트로델비와 다트로웨이 두 약제 모두 ADC 계열이지만 타겟과 페이로드 특성이 다르기 때문에 환자 특성에 따라 차별화된 접근이 필요하다"고 말했다.
이어 정 교수는 "(현재 발표된 데이터를 기반으로 볼 때)폐 기능이 저하된 환자라면 페이로드에 따른 폐독성 위험을 고려해 트로델비를, 종양 부하가 높아 빠른 반응이 필요한 환자라면 다트로웨이를 우선 고려할 수 있다"는 의견을 제시했다.
관련기사
- [ESMO 2025] '엔허투', HER2+ 조기 유방암에서 캐싸일라 능가
- [ESMO 2025]'키스칼리' 보조요법, 5년차에도 효과 유지
- [ESMO 2025] TIGIT 억제제 '돔바날리맙', 위암서 가능성 확인
- [ESMO 2025] '임핀지+FLOT', 수술 가능 위암서 전체생존 개선 입증
- [ESMO 2025] 지아이이노베이션, IL-2 면역항암제 성공 기대↑
- [ESMO 2025] '버제니오', CDK4/6 억제제 최초 OS 개선 입증
- 막 오른 'ESMO 2025'…종양학계 최신 이슈 한자리에
- [ESMO 2025] 퓨쳐켐 ‘루도타다이펩’, 반복 투여에도 안전성 입증
- [ESMO 2025] 이중항체 '이보네시맙', 폐암 1차 치료제 가능성 제시
- [ESMO 2025] 한미약품, 'EZH1/2 이중저해'로 고형암 정조준
- [ESMO 2025] 'AI 반응 예측' 루닛, 암 치료 글로벌 경쟁력 부각
- [ESMO 2025] 'FGFR2b', 진행성 위암 치료 표적으로 가능성 열려
- [ESMO 2025] 리가켐, ADC 임상 적용 가능성 입증
- [ESMO 2025]코오롱생명과학, '항암바이러스'로 항암제 개발 시동
- [ESMO 2025] 이뮨온시아, 'CD47·PD-L1'로 면역항암제 개발 가속화
- [ESMO 2025]셀랩메드, 'IL13Rα2' 타깃 CAR-T 1상 구두 발표
- [ESMO 2025]"다트로웨이, 면역치료 불가 삼중음성유방암 새 대안 제시"
- "키스칼리, 조기 유방암 완치 향한 장기 생존 견인"

