서울의대 임석아 교수, ESMO 2021서 VASTUS 연구의 1b상 결과 발표
일동홀딩스 계열사인 아이디언스가 개발 중인 표적항암제 후보물질 '베나다파립(venadaparib, 개발코드명 IDX-1197)'이 초기 임상시험 결과를 통해 차세대 PARP 억제제로서의 개발 가능성을 확인했다.
서울대학교병원 혈액종양내과 임석아 교수는 지난 16일 유럽종양학회 연례학술대회(ESMO 2021)에서 '베나다파립'의 1b상 임상시험인 VASTUS 연구 결과를 포스터 발표했다.
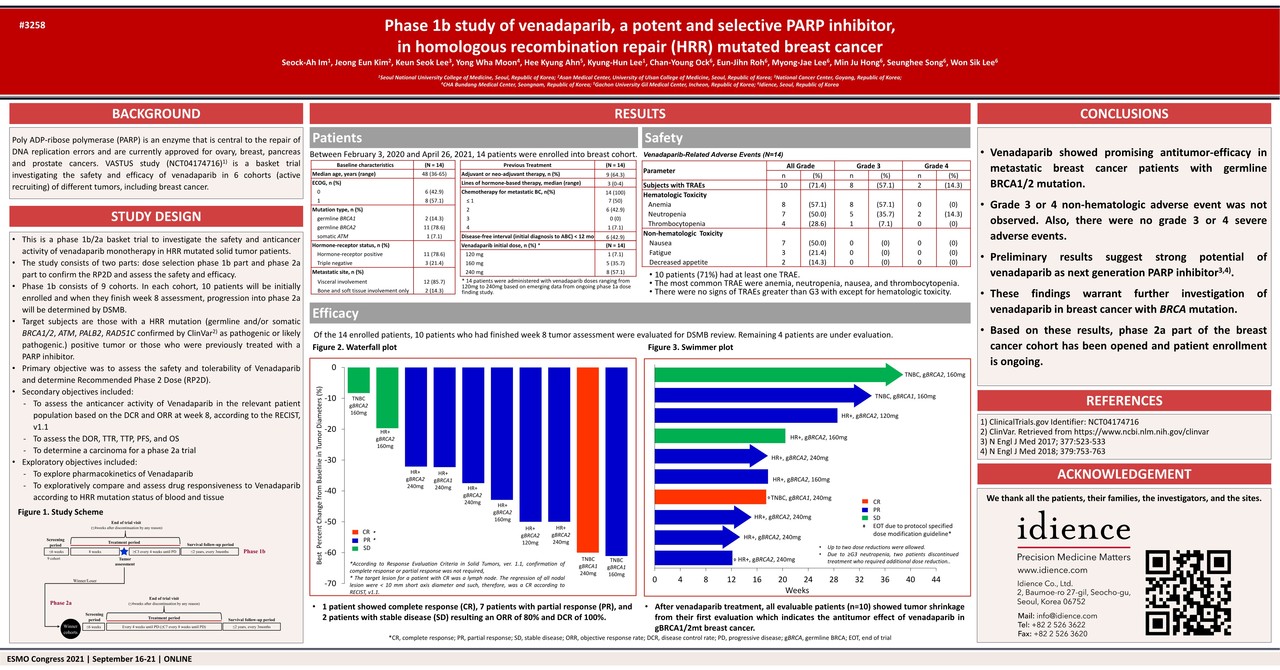
'상동 재조합 복구(Homologous recombination repair, HRR) 돌연변이 유방암에 대한 강력하고 선택적인 PARP 억제제, 베나다파립의 1b상 연구(원제: Phase 1b study of venadaparib, a potent and selective PARP inhibitor, in homologous recombination repair (HRR) mutated breast cancer)'란 제목으로 발표된 이번 포스터는 '베나다파립'이 현재 BRCA 변이 유방암 치료에 임상 실제를 바꿔버린(practice changing) 최초의 PARP 억제제 '올라파립'에 이어 차세대 PARP 억제제로서의 개발 가능성을 시사해 눈길을 끌었다.
VASTUS 연구는 유방암을 포함해 HRR 돌연변이를 가진 고형암 환자에서 '베나다파립' 단독요법의 안전성과 유효성을 평가한 1b/2a상 바구니형 임상시험(basket trial)으로, 연구 대상자는 HRR 돌연변이(병원성 생식기 혹은 체세포 BRCA1/2, ATM, PALB2, RAD51C) 양성이거나 이전에 PARP 억제제로 치료 경험이 있는 환자들이었다.
이번에 공개된 데이터는 2020년 2월 3일부터 2021년 4월 26일까지 유방암 코호트에 포함된 14명의 환자에서 얻은 안전성 및 유효성 평가 결과로, 참여 환자의 71%(10명)는 적어도 하나 이상의 치료 관련 이상반응을 나타냈지만, 혈액학적 독성을 제외한 3등급 이상의 치료 관련 부작용은 관찰되지 않은 것으로 나타났다.
즉, 기존 PARP 억제제의 주요 부작용인 중증(Grade 3)에 해당하는 오심, 피로, 식욕저하 등이 나타나지 않아, 차세대 약제로서의 안전성 개선을 시사한 것이다.
또한 14명의 환자 중 8주차 종양 평가를 마친 10명의 환자 데이터를 분석한 결과, 완전반응(1명) 및 부분반응(7명), 안정병변(2명)을 포함한 객관적반응률(ORR )이 80%로 나타났으며, 질병조절률(DCR)은 100%로 나타났다.
'베나다파립' 치료 후 10명의 환자 모두에서 종양 수축을 나타내며, gBRCA1/2 변이 유방암에서 '베나다파립'의 항종양 효과를 시사한 것이다.
이같은 결과에 따라 임석아 교수는 "베나다파립은 gBRCA1/2 변이가 있는 전이성 유방암 환자에서 유망한 항종양 효과를 보였으며, 3~4등급의 비혈액학적 이상반응은 물론 3~4등급의 심각한 부작용도 관찰되지 않았다"라며 "이번 예비 결과는 차세대 PARP 억제제로서 베나다파립의 강력한 잠재력을 시사한다"라고 말했다.
이어 "해당 결과는 BRCA 변이가 있는 유방암에서 베나다파립에 대한 추가 연구의 정당성을 뒷받침한다"며 "이를 바탕으로 유방암 코호트의 2a상 파트가 개설되었으며 현재 환자 등록이 진행 중"이라고 덧붙였다.

