UNIST 박성호 교수팀, 파골세포 분화 기전 발견
국내 연구진이 자가면역질환인 류머티즘성 관절염을 치료할 수 있는 실마리를 찾아냈다.
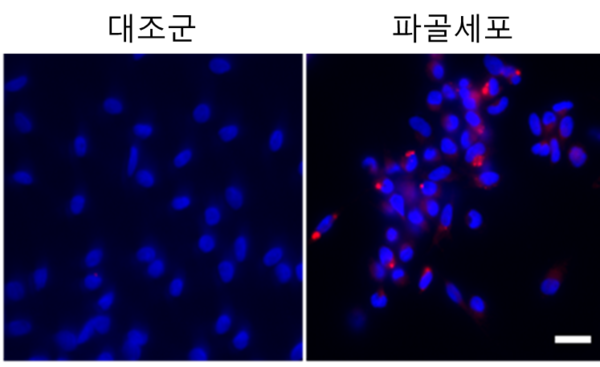
울산과학기술원(UNIST, 유니스트) 생명과학과 박성호 교수 연구팀은 10일 류머티즘성 관절염 환자의 관절부 뼈를 손상시키는 파골세포(Osteoclast) 형성과 분화에 관여하는 기전을 발견했다고 밝혔다.
연구팀은 효소 반응으로 뼈를 녹이는 파골세포의 분화 과정과 관련된 기전을 표적으로 한 치료 방법을 연구했다. 그 결과, 파골세포 형성에 영향을 미치는 중요한 인자로 알려진 NFATC1 유전자 근처에서 슈퍼인핸서(superenhancer)라는 후성유전학적 조절 요소를 발견했다.
인핸서(enhancer)는 DNA 서열 중 자신과 관련된 유전자에서 멀리 떨어진 곳에 있으면서 해당 유전자 발현 조절에 관여하는 부분을 말한다. 슈퍼인핸서는 인핸서가 높은 밀도로 모여 강한 세포 계통 특이성과 활성을 띠는 구조다.
NFATC1 슈퍼인핸서는 오직 파골세포에서만 형성됐으며 류머티즘성 관절염과 관련된 다른 세포에는 출현하지 않았다.
NFATC1 슈퍼인핸서 비암호화(non-coding) RNA 일종인 인핸서 RNA가 형성됐다. 비암호화 RNA는 단백질을 암호화하는 mRNA와 다르게 그 자체로는 단백질 아미노산 순서 정보를 담고 있지 않고 단백질도 만들어내지 않는 RNA 분자다. 비암호화 RNA는 자신과 관련된 유전자를 조절하는 기능을 갖고 있다. 특히 분자 서열 특이성 때문에 쉽게 치료 표적으로 삼을 수 있다는 게 연구팀 설명이다.
연구팀은 NFATC1 슈퍼인핸서 RNA가 없어지면 파골세포 분화 과정도 억제된는 현상을 확인했다. 이에 파골세포 분화 과정에서 형성되는 슈퍼인핸서 RNA를 치료 표적으로 활용 가능하다고 했다.
박 교수는 “이번 연구 결과가 류머티즘성 관절염 치료법 개발에 큰 진전이 될 것”이라고 말했다.
이번 연구결과가 담긴 논문 ‘RANKL-responsive epigenetic mechanism reprograms macrophages into bone-resorbing osteoclasts’는 국제학술지 ‘셀룰러 앤 몰리큘러 이뮤놀로지(Cellular and Molecular Immunology)’ 1월호에 출판될 예정이다.

