기존 PD-(L)1 기반 면역항암제 내성 환자 대상 효과 기대감
와이바이오로직스·에이비엘바이오 LAG-3 억제제 개발
신규 타깃 면역항암제인 LAG-3 억제제 개발에 속도가 붙고 있다. 국내외 개발 경쟁이 치열한 가운데 기존 PD-(L)1 면역항암제에 내성이 생긴 환자들에게 새로운 대안이 될 수 있을지 이목이 집중된다.
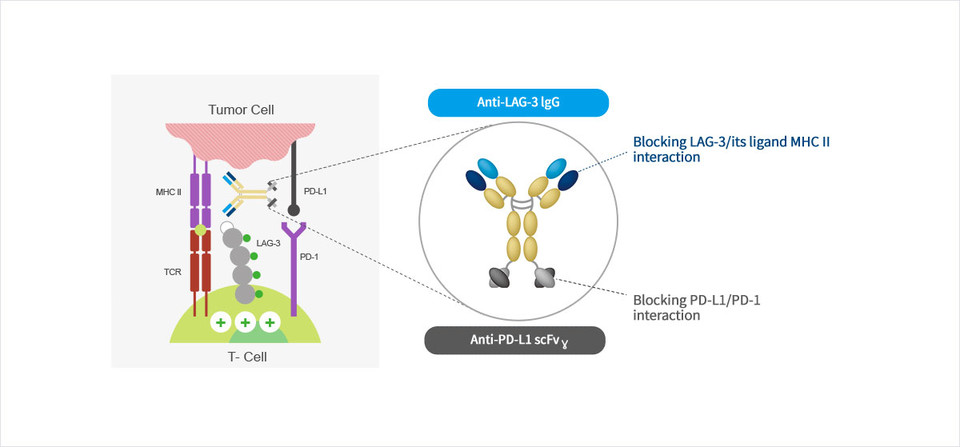
LAG-3는 활성화된 T세포에서 발현되는 단백질로, T세포의 활성화와 사이토카인 분비를 억제한다. 이 때문에 LAG-3 억제제 개발 기업들은 LAG-3 차단을 통해 T세포의 암세포 살상 기능을 회복시키는 동시에 사이토카인 분비를 줄일 수 있을 것으로 기대하고 있다.
현재 글로벌 제약사들이 앞 다퉈 LAG-3 억제제 개발을 진행하고 있으며, 속도에서 가장 앞선 곳은 BMS다.
BMS는 지난 9월 미국 식품의약국(FDA)으로부터 자사의 LAG-3 억제제 ‘렐라트리맙(Relatlimab)’에 대한 BLA 우선심사(Priority Review)를 승인받았다. FDA 우선심사는 신약승인 여부를 6개월 안에 결정짓는 제도로, 이에 따라 렐라트리맙 허가 여부는 2022년 3월까지 판가름 날 예정이다.
이밖에도 노바티스(렐라밀리맙), 베링거인겔하임(미프테나리맙), MSD(페브젤리맙), 리제네론(피안리맙) 등이 LAG-3 억제제 개발을 진행하고 있다. 주로 PD-1 억제제와의 병용투여가 이뤄지는 점이 특징이다.
노바티스는 자사의 PD-1 억제제 후보물질인 ‘스파르탈리주맙’과 병용요법 1/2상을 진행하고 있으며, 베링거인겔하임 역시 자사의 PD-1 억제제 후보물질 ‘BI754091’과 병용요법 1/2상을 이어가고 있다. MSD는 키트루다(성분명 펨브롤리주맙)와의 병용요법 1/2상을 진행하고 있다.
국내에서는 에이비엘바이오와 와이바이오로직스가 LAG-3 억제제를 개발하고 있다. 와이바이오로직스는 후보물질 'YBL-011'의 전임상을 진행 중인 것으로 알려졌다.
이 중 에이비엘바이오는 LAG-3 억제제 후보물질 ‘ABL501’ 개발에 속도를 내고 있다. 지난 6일 식품의약품안전처로부터 ABL501 1상 임상시험을 승인 받은 에이비엘바이오는 다음 날인 7일 삼성서울병원에서 첫 환자 투여를 진행했다. 임상시험 실시기관은 삼성서울병원을 포함해 서울대병원, 서울아산병원과 세브란스병원 등 총 4곳이다.
ABL501은 PD-L1과 LAG-3 두 타깃을 모두 억제하는 이중항체라는 점이 특징이다.
에이비엘바이오는 1상에서 고형암 환자(용량증량 코호트)를 대상으로 ABL501 단독요법 내약성 및 안전성을 평가하고 추후 용량 확장 코호트 및 병용요법 용량 증량 코호트를 추가할 예정이다.
이와 별개로 중국에서의 ABL501 개발 및 판매 권리를 보유한 파트너사 아이맵(I-Mab Biopharma)은 연내 중국에서 별도 임상을 개시할 계획이다. 지난 3분기 IND(임상시험계획)를 신청한 것으로 알려졌다.
에이비엘바이오 이상훈 대표는 “최근 글로벌 제약사들이 LAG-3 기반의 신약후보물질에 대한 유망한 연구결과를 내놓으면서 LAG-3가 주목할 만한 면역항암제 타깃으로 부상하고 있다"며 "임상을 통해 ABL501의 혁신신약 후보물질로서의 가능성을 규명해 LAG-3 치료제 개발을 주도해 나가겠다”고 말했다.

